Data Blitz A: Hautverbrennungen
Epidermale Stammzellen gehören zu den wenigen Stammzelltypen, die bereits bei der Behandlung von Patienten zum Einsatz kommen. Dank einer Entdeckung, die 1970 von Professor Howard Green in den USA gemacht wurde, können einem Patienten epidermale Stammzellen entnommen, vervielfältigt und dazu genutzt werden, um neue Epidermis im Labor zu züchten. Diese Epidermis kann dann als Hauttransplantat für den Patienten verwendet werden. Inzwischen ist es Forschern in einem Labor gelungen, aus den Zellen eines kleinen Hautstücks in nur drei Wochen bis zu 20 Hauttransplantate je 60 Quadratzentimeter Größe wachsen zu lassen. Da die neue Haut aus körpereigenen Zellen gezüchtet wurde, wird sie auch nicht abgestoßen. Die Technik wird hauptsächlich eingesetzt, um das Leben von Patienten zu retten, die großflächige Verbrennungen dritten Grades erlitten haben. Nur eine Handvoll klinischer Zentren sind in der Lage, diese kostspielige Behandlung erfolgreich durchzuführen. Allerdings ist es keine ideale Lösung. Mit dieser Methode kann ausschließlich die Epidermis ersetzt werden; die neue Haut besitzt keine Hautanhangsgebilde, wie Haarfollikel, Schweißdrüsen oder Talgdrüsen. Besonders das Fehlen der Schweißdrüsen beeinträchtigt die Patienten, denn sie haben somit keine normale Thermoregulation. Es wird intensiv daran geforscht, die Eigenschaften der gezüchteten Haut zu verbessern.
Lesen Sie weiter: Hautstammzellen: Woher kommen sie und was können sie
Data Blitz B: Leberversagen
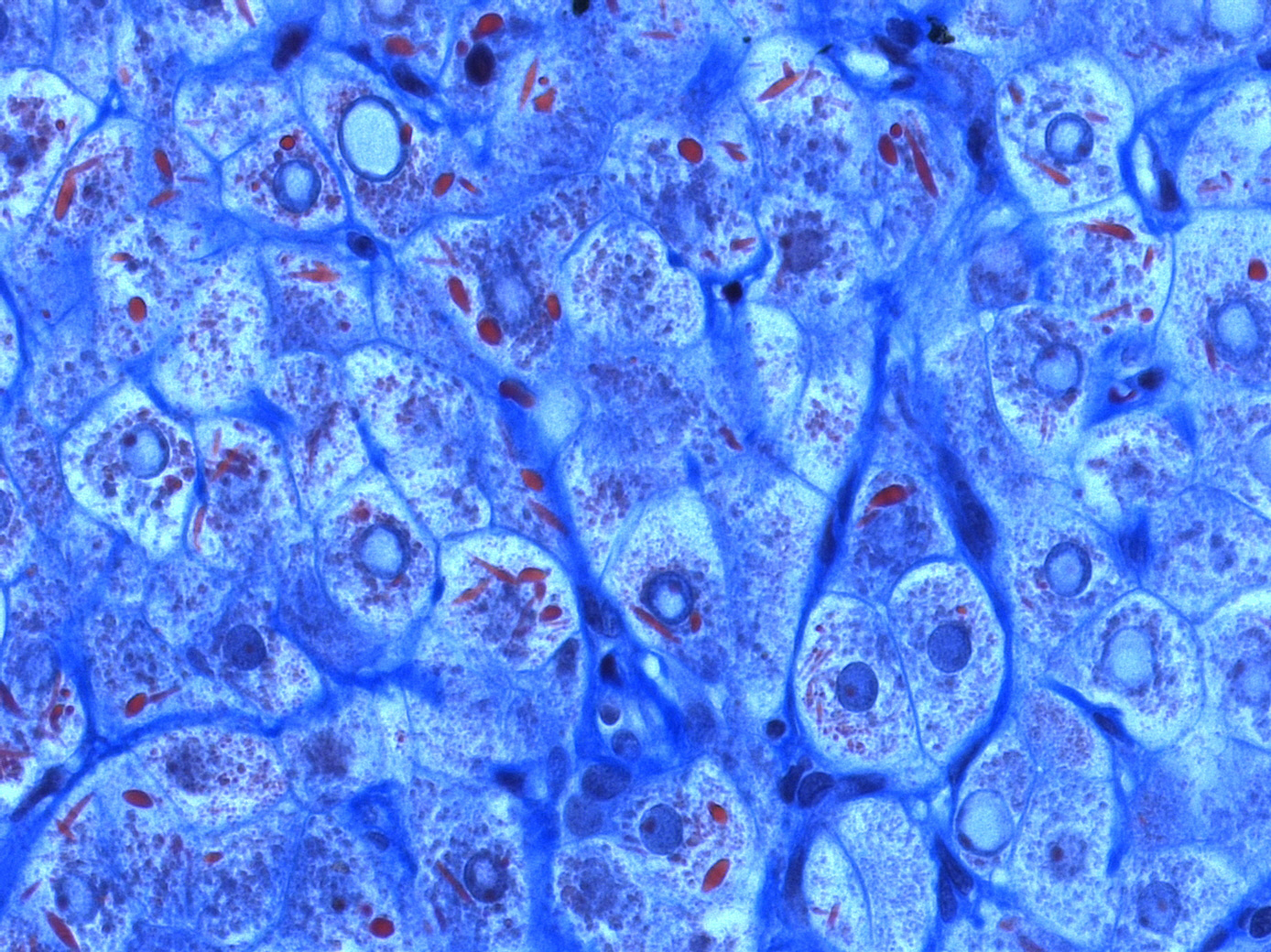 Abbildung: Mega-Mitochondrien in Leberzellen (Hepatozyten) im Lichtmikroskope (Färbung mit Chromotrop-Anilinblau ((CAB)
Abbildung: Mega-Mitochondrien in Leberzellen (Hepatozyten) im Lichtmikroskope (Färbung mit Chromotrop-Anilinblau ((CAB)
Bildnachweis: Alexquaas/Wikimedia
Lange war die Lebertransplantation die einzige Therapiemöglichkeit bei akutem Leberversagen. Das soll sich bald ändern – dank Stammzelltherapie. Leberzellen (Hepatozyten) aus dem Labor können zur Überbrückung eingesetzt werden. Dazu wird die natürliche Leberausbildung genau erforscht, um sie auf die Leberzellzüchtung übertragen zu können. Wachstumsstoffe (Zytokine) werden hinzugegeben und Reagenzien entwickelt, die Zelleigenschaften der Genexpression feinregulieren. Auch Mikro-RNAs, also nicht codierende RNA-Moleküle, können dabei eine wichtige Rolle spielen. Der Vorteil des Verfahrens: Es werden patienteneigene Zellen verwendet sodass keine immunsupprimierenden Medikamente notwendig sind. Es wird auch daran geforscht, körpereigene Bindegewebszellen in der Leber so in Hepatozyten umzuwandeln, dass diese an dem Heilungsprozess teilnehmen.

Erfahren Sie mehr: GSCN Kurzfilm - Die Leber: Therapie mit Stammzellen -
Die Forschung von Prof. Michael Manns und Prof. Tobias Cantz (MH Hannover)
Lesen Sie weiter: Chronische Lebererkrankung: Wie könnte Regenerative Medizin helfen?
Data Blitz C: Hornhauttrübung
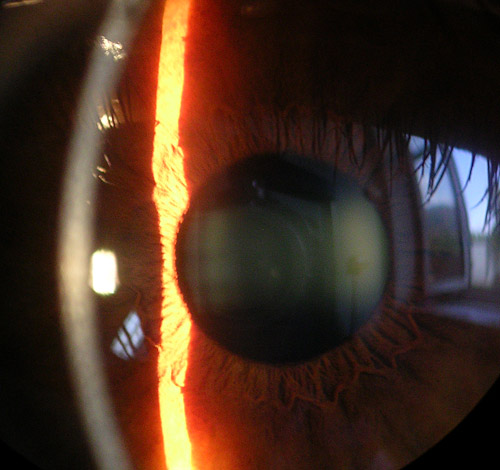 Abbildung: Aufnahme der Hornhaut, Iris und Linse mit einer Spaltlampe
Abbildung: Aufnahme der Hornhaut, Iris und Linse mit einer Spaltlampe
Bildnachweis: Baristoprak~commonswiki/Wikimedia
James Funderburgh von der Universität Pittsburgh hat zusammen mit Augenärzten aus Indien untersucht, ob Stammzellen genutzt werden können, um Hornhautverletzungen zur Abheilung zu bringen. Für ihre Experimente verwendeten sie ursprünglich die Limbusstammzellen von verstorbenen Menschen. Der Limbus ist die Übergangszone zwischen Horn- und Lederhaut des Augapfels. Für die heutigen klinischen Anwendungen werden die Zellen vom Limbus des gesunden Auges der Patienten entnommen. Eine solche Biopsie kann nach Aussage der Forscher so klein gehalten werden, dass sie das gesunde Auge nicht gefährdet. Die Zellen werden dann zunächst im Labor vermehrt, was heute problemlos möglich ist. An Mäusen haben die Forscher, die die Stammzellen anschließend mit einem Fibrinkleber direkt auf die verletzte Hornhaut aufgebracht. Wie Funderburgh berichtet, bildeten sich nach der Behandlung die Narben auf der Hornhaut zurück. Die Transparenz sei innerhalb von vier Wochen zurückgekehrt und die Tiere könnten jetzt wieder sehen. Zu diesen Behandlungsmöglichkeiten gibt es inzwischen auch das Präparat „Holoclar“ auf dem europäischen Markt.
Lesen Sie weiter:
- Ärzteblatt 12/2014 (Quelle)
- Das Auge und Stammzellen: Auf dem Weg zur Behandlung von Blindheit
- Europa lässt Holoclar zu, das erste Stammzellforschung-basierte medizinische Produkt (EN)
Data Blitz D: Leukämie
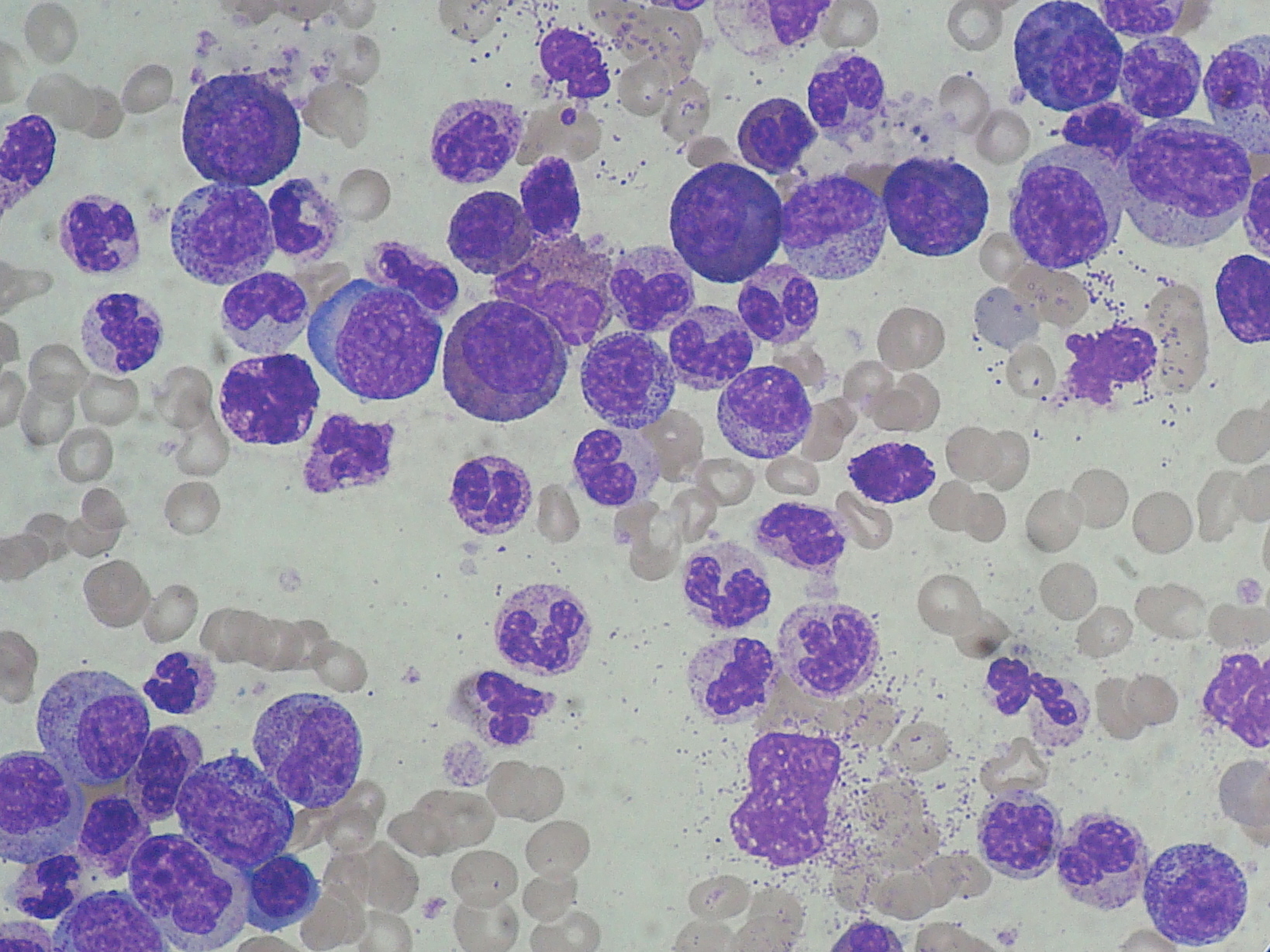 Abbildung: Chronische myeloide leukämie (CML): starke Leukozytose mit Linksverschiebung der Granulozyten
Abbildung: Chronische myeloide leukämie (CML): starke Leukozytose mit Linksverschiebung der Granulozyten
Bildnachweis: Paulo Henrique Orlandi Mourao/Wikimedia
Bei Leukämie haben die Blutstammzellen ihre Fähigkeit der Selbsterneuerung verloren. Die Zellen erneuern sich ohne sich zu Spezialisten zu entwickeln. Die Leukämiezellen produzieren weiße Vorläuferzellen, die nicht ausreifen und nicht funktionstüchtig sind. Sie breiten sich im Knochenmark aus und stören die normale Blutbildung. Mit der Folge, dass das Blut nicht mehr genug Sauerstoff transportiert und seine Funktion der Wundheilung verliert. Zur Behandlung von Leukämie werden Blutstammzellen transplantiert. Dabei werden die körpereigenen Blutstammzellen mit allen blutbildenden Zellen durch hohe Dosen von Chemotherapeutika oder Bestrahlung vernichtet. In einem zweiten Schritt werden die Blutstammzellen vom Patienten, die vorab gewonnen wurden, zurückgegeben (autolog) oder Blutstammzellen von einem passenden Spender (allogen) transplantiert. Die allogene Stammzelltransplantation ist notwendig, wenn die Leukämie in den patienteneigenen Blutstammzellen entstanden ist. Sie birgt die Gefahr einer Transplantat-gegen-Wirt-Erkrankung (Graft-versus-Host Diesease, GvHD), bei dem die Immunzellen des Spenders die Organe des Patienten angreifen.

Erfahren Sie mehr: GSCN Kurzfilm über die Zelltherapie mit CRISPR/Cas -
Die Forschung von Hubert Serve (Universitätsklinikum Frankfurt)
Lesen Sie weiter: Leukämie: wie können Stammzellen helfen?
Data Blitz E: Diabetes
Douglas Meltons Kinder haben Diabetes und müssen Insulin spritzen. Das will der international bekannte Harvard-Professor ändern.
Aus der Neuen Zürcher Zeitung, 07.10.16:
„«Bei Diabetes Typ 1 fehlt nur ein einziger Zelltyp, der noch dazu eine absolute Spezialaufgabe in seinem Organ, dem Pankreas, ausübt: den Blutzuckerspiegel messen und bei Bedarf Insulin ausschütten. Das muss sich doch durch im Labor gezüchtete Ersatzzellen heilen lassen», war Melton schon damals überzeugt. Also machte er sich daran, diese Ersatzzellen zu züchten. (...)
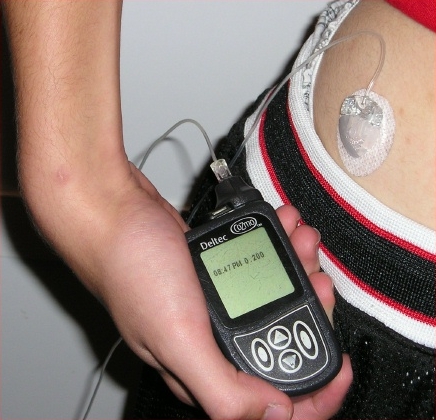
Abbildung: Insulin Pumpe mit Infusionsgerät
Bildnachweis: mbbradford/Wikimedia
Es sollte bis 2014 dauern, bis das Team in Harvard es schaffte, aus embryonalen Stammzellen wie auch aus iPS-Zellen funktionsfähige Betazellen herzustellen – der ersehnte Durchbruch. Die gezüchteten Betazellen messen Glukosekonzentrationen, produzieren Insulin und geben es bei Bedarf ab. Dies klappt sowohl in der künstlichen Umgebung einer Petrischale als auch in diabetischen Mäusen. Auch anderswo auf der Welt arbeiteten Forscher an diesem Ziel, schneller als Melton war niemand. Manche versuchen auch, Zellen direkt in der Bauchspeicheldrüse zu Betazellen umzuprogrammieren.
«Es gibt im Körper mindestens 70 Eiweiße, die die Entwicklung und Spezialisierung von Körperzellen aus embryonalen Stammzellen steuern. Wir mussten diejenigen finden, die Betazellen entstehen lassen, und das in der richtigen zeitlichen Kombination und Konzentration», beschreibt Melton die größte Hürde.
Auch andere Fragen sind noch offen. So ist noch unklar, ob iPS- oder embryonale Stammzellen das bessere Ausgangsmaterial darstellen. Für standardisierte Therapien werden sich vermutlich Letztere durchsetzen, da man dort einmal eine Stammzelllinie und die daraus gezüchteten Betazellen durch alle Sicherheitschecks schicken und sie danach für jeden Patienten verwenden kann. Bei der Verwendung von iPS-Zellen, welche von dem zu behandelnden Patienten stammen, müssten die Sicherheitstests für jeden Patienten einzeln erfolgen – für die klinische Anwendung zu aufwendig und teuer.
Zudem weiß man noch nicht, wie viele neu gezüchtete Betazellen man zur Kontrolle des Blutzuckerspiegels benötigt und wie lange diese im Körper funktionieren. Antworten auf solche Fragen könnte der Ende 2014 von der kalifornischen Firma ViaCyte gestartete, weltweit erste Therapieversuch mit Ersatzzellen für Diabetiker geben. Dabei wurden einigen Patienten aus Stammzellen gezüchtete und in Kapseln aus Biopolymeren verpackte Vorstufen von Betazellen implantiert. Erste Ergebnisse zeigen laut der Firma, dass zumindest manche der implantierten Zellen nach 12 Wochen reif sind. Wie gut sie funktionieren und wie lange sie überleben werden, ist noch ungewiss.“
Lesen Sie weiter:
- Neue Zürcher Zeitung, 10/16, Stephanie Lahrtz: Ein Vater forscht für seine Kinder
- Diabetes: Wie könnten Stammzellen helfen?
Data Blitz F: Parkinson
Ärzte und Wissenschaftler sind der Ansicht, dass eine Zellersatztherapie auch bei der neurodegenerativen Erkrankung Parkinson funktionieren kann, und berufen sich dabei auf die Ergebnisse von Transplantationsstudien, die in den 1980er Jahren durchgeführt wurden. Skandinavische Wissenschaftler hatten bei vier Parkinson-Patienten Zellen aus den Nebennieren in das Gehirn verpflanzt. Die Nebennieren sitzen auf den Nieren und enthalten Zellen, die Dopamin und ähnliche Substanzen produzieren. Nach der Transplantation trat im Zustand der Patienten eine gewisse Besserung ein, die jedoch gering war und nicht lange anhielt. Dies war die erste Transplantation von Dopamin-produzierendem Gewebe in das menschliche Gehirn. Bei späteren Versuchen transplantierten Wissenschaftler aus Schweden, den USA und Kanada Dopamin-produzierende Neuronen von menschlichen Föten in Tiere und in Patienten und erzielten damit teils wesentliche, teils jedoch nur mäßige Verbesserungen. In einer Patientengruppe kam es zu Nebenwirkungen und in einigen Fällen ging die Krankheit mehr als ein Jahrzehnt nach dem Eingriff auch auf die transplantierten fetalen Zellen über.
.jpg)
Abbildung: Lichtmikroskopische Aufnahmen in verschiedenen Vergrößerungen der Substantia nigra eines Parkinson Patienten mit Lewy Körperchen und Lewy Neuronen (Färbung für alpha synuclein und Hämatoxylin)
Bildnachweis: Suraj Rajan/Wikimedia
Nach wie vor hoffen die Wissenschaftler, dass man den Beginn der Parkinson-Krankheit hinauszögern oder ihr Fortschreiten verlangsamen kann, indem man Zellen aus frühen Entwicklungsstadien des Menschen in das Gehirn einbringt. Es steht jedoch nicht genug fetales Gewebe zur Verfügung, um die große Zahl an Parkinson-Patienten zu behandeln. Zudem wirft die Verwendung von Föten ethische Fragen auf. Stammzellen könnten als alternative Quelle neuer Zellen für Parkinson-Patienten dienen.
Embryonale Stammzellen (ES-Zellen) könnten dazu gebracht werden, Dopamin-produzierende Neuronen zu bilden, die man den Patienten transplantieren würde. Im Labor hat man Dopamin-produzierende Neuronen sowohl aus embryonalen Stammzellen von Mäusen als auch von Menschen hergestellt. Induzierte pluripotente Stammzellen (iPS) könnten im Labor aus ausdifferenzierten Hautzellen der Patienten hergestellt und dann zur Bildung Dopamin-produzierender Neuronen verwendet werden. 2010 behandelten amerikanische Wissenschaftler Ratten mit Neuronen, die mittels iPS-Verfahren aus menschlichen Hautzellen hergestellt worden waren. Die transplantierten Neuronen bewirkten bei den Ratten eine Verringerung der Parkinson-Symptome. Mäuse und Ratten brauchen jedoch weniger Neuronen als Menschen und es bleibt fraglich, ob dieser Ansatz beim Menschen funktioniert. Zudem sind weitere Studien erforderlich, um zu belegen, dass die Behandlung mit den Zellen sicher ist und keine Tumore im Gehirn verursacht.
Lesen Sie weiter: Parkinson: Wie können Stammzellen helfen?