HeLa-Zellen
HeLa-Zellen werden seit den 50er-Jahren in der Forschung eingesetzt. Es handelt sich um eine ständig vermehrbare Zell-Linie, die sich zum Beispiel sehr gut zur Erprobung des Polio-Impfstoffes eignet. Die Zell-Linie wird mittlerweile kommerziell vertrieben und für viele Experimente genutzt. Auf wissenschaftlichen Erkenntnissen aus Experimenten mit HeLa-Zellen basieren weltweit tausende angemeldete Patente.
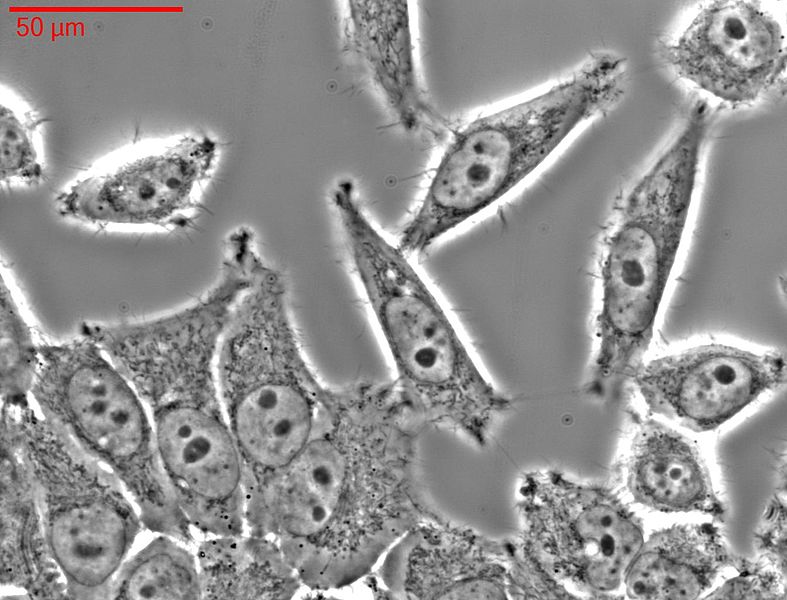
Abbildung: HeLa-Zellen im Lichtmikroskop
Bildnachweis: Fraunhofer IBMT - Anastasiadis, Weiß/Wikimedia
Diese Zell-Linie und ihr Name haben eine besondere Geschichte: Henrietta Lacks war eine Patientin am Johns-Hopkins-Hospital in Baltimore. 1951 wurde sie dort wegen eines Gebärmutterhals-Tumors behandelt. Das John-Hopkins-Hospital war zu diesem Zeitpunkt eines der wenigen Krankenhäuser, das auch afroamerikanische Patienten behandelte. Oft wurde dafür ein stillschweigendes Einverständnis in Studienteilnahmen vorausgesetzt. Henrietta Lacks´ Gynäkologe Howard W. Jones entnahm eine Zellprobe des Tumors. Er übergab sie an den Zellforscher George Otto Gey, der daraus die potenziell unsterbliche HeLa-Zell-Linie entwickelte. In Anlehnung an den Namen der Patientin Henrietta Lacks nannte er sie HeLa-Zellen. Henrietta Lacks wurde nie über die Verwendung ihrer Zellen informiert. Auch ihre Familie erfuhr erst Jahre später von der Verwendung der Zellen. Auszüge aus Henriettas Patientenakte wurden ohne Einwilligung der Familie veröffentlicht. 2013 wurde ihre Genomsequenz entschlüsselt und in eine frei zugängliche Datenbank aufgenommen. Dies löste eine weltweite Debatte aus. Erst danach wurde eine Vereinbarung mit den Nachkommen von Henrietta Lacks getroffen, welche die Verwendung der Daten regelt. Zwei Familienmitglieder haben heute Sitze in einem Komitee, das über den Zugang zu dem DNA-Code entscheidet.
 Abbildung: Gedenktafel für Henrietta Lacks in Clover, Virginia
Abbildung: Gedenktafel für Henrietta Lacks in Clover, Virginia
Bildnachweis: Emw/Wikimedia
Informierte Einwilligung
In medizinische Behandlungen müssen Patienten einwilligen. Das gilt auch für die Nutzung ihrer Zellen für die Forschung. Mit „informierter Einwilligung“ ist gemeint, dass der Patient sich in einem Zustand befindet, in dem er in der Lage ist, die Entscheidung selbstbestimmt zu treffen. Der juristische Begriff dafür ist "Einwilligungsfähigkeit". In Ausnahmen kann auch ein Bevollmächtigter diese Einwilligung geben.
Der Wissenschaftler hat zudem eine Aufklärungspflicht. Erst wenn der Patient aufgeklärt wurde, kann er eine informierte Einwilligung geben.
Die informierte Einwilligung taucht schon am Anfang des 20. Jahrhunderts als forschungsethisches Prinzip auf. Trotzdem wurde immer wieder dagegen verstoßen.
Erst 1964 verabschiedete der Weltärztebund die informierte Einwilligung in ihren ethischen Grundsätzen für medizinische Forschung am Menschen bei seiner Generalversammlung in Helsinki – auch aufgrund der Gräueltaten nationalsozialistischer Mediziner an jüdischen Gefangenen. Das Dokument heißt deshalb Helsinki-Deklaration.